Soluciones de alimentación para uso médico: las normas brindan seguridad
2018-07-26
Las personas y la alimentación no son compatibles, y esto es especialmente cierto cuando las personas son pacientes, ya sea en un centro médico o, cada vez más, en un entorno hogareño. Con el fin de garantizar la seguridad de los pacientes y los profesionales de la salud, el negocio de la atención médica está fuertemente regulado por una serie de requisitos basados en normas y pruebas de productos asociadas.
Lo más importante del régimen de normas es la IEC 60601, que se compone de un conjunto de requisitos específicamente para los equipos eléctricos y electrónicos utilizados en el área de la salud. Publicada originalmente hace unos 40 años, la IEC 60601 se ha mantenido al día con los cambios de la industria.
En este artículo técnico, examinamos algunos de los principios más importantes de la IEC 60601 en lo que respecta a la implementación de la fuente de alimentación, así como algunos de los nuevos requisitos, como la necesidad de una evaluación de riesgos. Además, se revisarán las formas prácticas para lograr la conformidad, como la asistencia disponible para los fabricantes de dispositivos de uso médico.
Introducción
Una de las principales preocupaciones de seguridad con respecto a los dispositivos de uso médico es que, por lo general, el paciente está conectado al dispositivo por medio de electricidad. Por ejemplo, las almohadillas conductoras de un electrocardiógrafo. En la IEC 60601 se definen como “partes aplicadas” (AP) y se consideran importantes dentro de la norma cuando se definen los requisitos generales de un producto médico.
Los dispositivos de uso médico deben incorporar al menos un medio de protección (MOP) para garantizar que tanto el paciente, si está conectado a través de AP, como el operador están protegidos de los riesgos de una descarga eléctrica, incluso si ocurriese una falla. Se puede lograr un MOP a través de un aislamiento de seguridad, una tierra de protección, una distancia de fuga definida, un entrehierro, otras impedancias de protección o mediante la implementación de estas técnicas combinadas.
En la norma, los operadores y los pacientes se tratan de manera diferente, por lo que se clasifica en "Medios de protección del operador" (MOOP) y "Medios de protección del paciente" (MOPP). Una razón para esta diferencia es que el paciente puede estar conectado físicamente a través de una AP y estar inconsciente cuando ocurre la falla. Debido a este riesgo, los requisitos de MOPP son los más estrictos de los dos. Cada término se define según el voltaje de aislamiento, la distancia de fuga y el nivel de aislamiento.
|
||||||||||||||||||||||||
Figura 1: Definiciones de MOOP y MOPP para la IEC 60601 (Fuente de la imagen: TRACO Power)
Las normas que evolucionan
La IEC 60601 ha evolucionado desde que se publicó hace casi 40 años. Como las fuentes de alimentación y los módulos no son dispositivos de uso médico en sí mismos, las normas no se aplican directamente a ellos. Sin embargo, los fabricantes de dispositivos de uso médico no podrían lograr el cumplimiento de las normas sin soluciones de alimentación que hayan sido diseñadas con las aplicaciones de uso médico en mente.
Hasta hace poco, se podía suponer que los dispositivos de uso médico se utilizarían exclusivamente en instalaciones médicas especializadas, como hospitales y clínicas. Dichas instituciones proporcionaban alimentación limpia exclusiva para el uso de los dispositivos médicos más sensibles. En la actualidad, los pacientes exigen comodidad e instalaciones médicas con recursos limitados, lo que significa que los dispositivos de uso médico se utilizan cada vez más en el hogar. Cuestiones como la compatibilidad electromagnética (EMC) son cada vez más importantes aquí debido a la prevalencia de tecnologías como Bluetooth y Wi-Fi. Debido a esto, la última versión de la norma (4.ª edición) ha cambiado los procedimientos de prueba y los niveles de aceptación para EMC.
Otra introducción significativa ha sido el requisito para realizar una evaluación de riesgos de acuerdo con la ISO 14971. La gestión de riesgo se considera un componente clave para demostrar el cumplimiento normativo de los dispositivos de uso médico, y la norma ISO 14971 define las mejores prácticas para todas las etapas del ciclo de vida útil de estos dispositivos.
La Directiva de Dispositivos Médicos agrega todavía más requisitos y exige a los fabricantes implementar un Sistema de gestión de calidad (QMS) que cumpla con la norma ISO 13485. El requisito principal es que una organización (como un fabricante de suministro de energía) pueda demostrar la capacidad para cumplir con los requisitos de las normas y del cliente de forma constante.
Con aprobación médica, los convertidores de CC/CC con calificación 2 x MOPP proporcionan flexibilidad
El enfoque característico para lograr el cumplimiento de la IEC 60601 es utilizar una fuente de alimentación de CA/CC que esté aprobada para el uso médico. Sin embargo, las aplicaciones con calificación BF también requieren que el instrumento AP cumpla con la clasificación 2 x MOPP. En la actualidad, muchas de las fuentes de alimentación de CA/CC en el mercado aprobadas para uso médico no tienen una clasificación 2 x MOPP y no son aptas como una solución de energía independiente para aplicaciones donde se requiere el cumplimiento de BF. En estos casos, un convertidor de CC/CC con clasificación 2 x MOPP, aprobado por la IEC 60601, será compatible con BF para la AP. Otro ejemplo común son los dispositivos de uso médico que implementan una capacidad de respaldo de batería y deben cumplir con la clasificación 2 x MOPP durante la falla de CA.
Los dispositivos de uso médico a menudo requieren de varios voltajes de CC que impulsen el instrumento AP de diferente voltaje de CC del sistema principal proporcionado. Para evitar el suministro de una fuente de alimentación de CA/CC personalizada, se pueden combinar convertidores de CC/CC con clasificación 2 x MOPP, IEC 60601, junto con, por ejemplo, una fuente de alimentación de CA/CC ITE 60950. En otras ocasiones, la confianza en la ingeniería simplemente se plantea mediante la garantía de utilizar convertidores de CC/CC de calidad médica 2 x MOPP para el instrumento AP, incluso cuando la fuente de alimentación de CA/CC seleccionada cuenta con la aprobación IEC 60601.
Los requisitos principales para 2 x MOPP (Figura 1) son el aislamiento de 4000 V deCA, la distancia de fuga de 8 mm y el aislamiento doble. La mayoría de los convertidores de CC/CC disponibles (incluidos los que cuentan con la aprobación EN60950) ofrecen entre 500 V deCC hasta alrededor de 1600 V deCC de aislamiento y, por lo tanto, no son adecuados para aplicaciones de uso médico. Sin embargo, hay disponibles convertidores de CC/CC especializados que cumplirán con los requisitos de AP cuando se utilicen junto con dichas fuentes de alimentación estándar.
Al proporcionar hasta 5000 V deCA de aislamiento, doble aislamiento y 8 mm de distancia de fuga a través de su transformador de aislamiento galvánico, un convertidor de CC/CC todavía puede proteger al paciente en caso de falla de la fuente de alimentación principal de CA/CC, evitando así los niveles de voltaje de red que aparecen en cualquier punto AP del paciente.
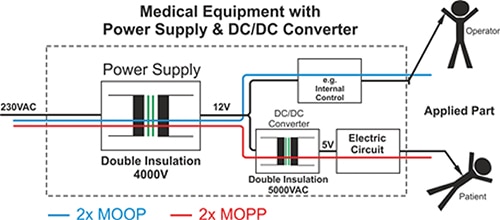
Figura 2: Uso de convertidor de CC/CC para lograr protección 2 x MOPP. (Fuente de la imagen: TRACO Power)
El enfoque de TRACO para soluciones de energía seguras de uso médico
En el fondo del enfoque de TRACO para acercar soluciones de alimentación de primera categoría para la industria médica se encuentra la tecnología de transformadores. Desarrollado y perfeccionado durante un largo período, su enfoque exclusivo garantiza la separación y el aislamiento requeridos, al tiempo que logra un acoplamiento suficiente para permitir que el convertidor de CC/CC funcione de manera eficiente.
Una baja capacitancia de acoplamiento entre los devanados de transformador primarios y secundarios es un aspecto importante de la implementación de la protección. Los valores tan bajos como 10-15 pF aseguran que haya una transferencia de corriente insignificante a través de la barrera de aislamiento, proporcionando protección al paciente de acuerdo con los requisitos de la norma IEC 60601.
TRACO también implementa el QMS de acuerdo con ISO 13485, que cubre tanto el diseño como los procesos de fabricación. Además, las prácticas adicionales que superan los requisitos de las normas garantizan altos niveles de calidad y seguridad dentro de los productos.
Los componentes de grado industrial se seleccionan y obtienen para garantizar la robustez del producto final. Como resultado, los dispositivos diseñados para el uso en equipos de TI quedan excluidos por políticas internas de TRACO. La mano de obra está garantizada mediante el cumplimiento de la norma internacional IPC-A-610, en la que TRACO opera en el nivel 3, el nivel más alto de mano de obra. Estas medidas combinadas le permiten a TRACO ofrecer garantías de productos de hasta 5 años en algunos de ellos.
Como fabricante de soluciones de energía en lugar de dispositivos de uso médico, TRACO no está obligado a proporcionar datos de evaluación de riesgos. Sin embargo, TRACO cumple con la norma ISO 14971 y proporciona archivos de evaluación de riesgos que cubren áreas cruciales como la ruptura del aislamiento, el uso mientras se invierte, los efectos de la falla del ventilador, la inflamabilidad, el choque mecánico y mucho más para los clientes. El suministro de estos datos contribuye de manera significativa a la evaluación de riesgos de los productos de uso médico finales de los clientes, ahorrándoles tiempo y dinero durante el proceso de diseño.
Una oferta integral de productos
TRACO ofrece soluciones de CA/CC y CC/CC para aplicaciones de uso médico, las cuales cumplen con los requisitos de 2 x MOPP. Cumplen con los requisitos EMC de IEC 60601-1 (4.ª edición) y son adecuadas para todos los dispositivos de uso médico de piezas aplicadas y conectados al paciente (conforme a BF). Los productos de CA/CC abarcan pequeños módulos de montaje en PCB de 5 W, una gama de diseños de armazón abierto de potencia media y fuentes de alimentación cerradas que ofrecen niveles de potencia de hasta 450 W.

Figura 3: La serie TPP 40 de TRACO está disponible tanto en armazón abierto como cerrado. (Fuente de la imagen: TRACO Power)
Todas las PSU ofrecen entrada de red universal (de 85 a 264 V deCA/de 120 a 370 V deCC) con corrección de factor de potencia (PFC) activa superior a 100 W. El rango comprende salidas individuales, dobles y triples, que cubren casi todos los requisitos de la aplicación
La gama de convertidores de CC/CC de TRACO comprende módulos de montaje en PCB con niveles de potencia de 2 W a 30 W. Los dispositivos ofrecen rangos de entrada de 2:1 y 4:1 con entradas nominales de 5 V, 12 V, 24 V y 48 V disponibles. Las salidas simples y duales se ofrecen de 3.3 V deCCa ± 15 V deCC.

Figura 4: La serie THM de 15 vatios es un convertidor de CC/CC de uso médico de montaje en PCB. (Fuente de la imagen: TRACO Power)
Todos los convertidores de CC/CC aprobados para el uso médico de TRACO ofrecen 5000 V de CA rms de aislamiento de entrada-salida que está clasificado para una tensión de trabajo de 250 V de CA rms. Esto, junto con las corrientes de fuga por debajo de 2 μA, los convierte en opciones ideales para usar junto con las PSU de CA/CC no aprobadas en aplicaciones de uso médico de seguridad crítica.
Resumen
El mercado de la salud está creciendo y cambiando rápidamente; y las normas aplicables, como la IEC 60601, evolucionan constantemente para mantenerse al día. Los fabricantes de dispositivos de uso médico son los responsables en última instancia de garantizar la seguridad de los pacientes y los operadores de los productos. Sin embargo, al asociarse con proveedores experimentados de suministro de energía, los desafíos y riesgos pueden reducirse significativamente. Al aprovechar el equipo de TRACO, dichos fabricantes obtienen acceso a productos de alta calidad, confiables y seguros, junto con un soporte integral y experto en lo que respecta a los estándares médicos actuales.
Descargo de responsabilidad: Las opiniones, creencias y puntos de vista expresados por los autores o participantes del foro de este sitio web no reflejan necesariamente las opiniones, las creencias y los puntos de vista de DigiKey o de las políticas oficiales de DigiKey.




